11月中旬,三叶草生物在上海举办了“呼吸道合胞病毒(RSV)疫苗企业交流会”,现场超一百多位机构投资者和多家国内券商分析师团队参加了此次线下交流活动。活动中,三叶草生物首次公布了其RSV PreF候选疫苗SCB-1019亮眼的临床前数据,表示其“正加速在中国和全球推动SCB-1019疫苗的临床申报和开发,公司预计2024年上半年进入临床Ⅰ期”;今天,三叶草生物公布,公司 RSV PreF - 三聚体亚单位候选疫苗(SCB-1019)的Ⅰ期人体临床试验中,首批受试者已完成入组,公司正式启动 RSV候选疫苗Ⅰ期临床试验,这就是三叶草速度!
呼吸道合胞病毒(RSV)是全球主要致死病因之一,其感染导致的疾病负担沉重,且易感染的高风险人群是“老年人”和“婴幼儿群体”。尤其在老年人(≥60岁)群体,感染呼吸道合胞病毒后可能引发慢阻肺、充血性心力衰竭等严重并发症,死亡率高达8%;而目前RSV感染长期缺乏有效的防治手段,老年人等脆弱人群感染后的治疗方法以对症治疗和广谱抗病毒治疗为主,亟需安全高效的RSV疫苗预防感染。
然而人类RSV疫苗的研发史长达70余年,屡败屡战,RSV疫苗的开发难度可见一斑。直至今年5月美国药监局 (FDA) 才首次批准两款RSV疫苗,分别来自GSK和辉瑞,这两款重组蛋白路线的RSV疫苗获批后的第一个商业化季度市场表现远超业界预期,总计季度销售额超过10亿美金。这样的市场表现,不仅力证了该领域的疾病负担和市场需求,也能解释为何国内市场已有一批药企的研发都向RSV赛道倾斜。国内目前尚无获批上市的RSV疫苗,根据公开资料,研发方面目前进入临床阶段的有艾棣维欣以及三叶草生物。艾棣维欣采用G蛋白亚单位疫苗,而三叶草生物则应用其创新独有的全人源蛋白质三聚体化(Trimer-Tag)技术平台和已申请专利的高度稳定的PreF突变,构建出二价重组蛋白RSV候选疫苗SCB-1019,其包含两个稳定融合前构象的F抗原(A和B亚型RSV F蛋白)。
业界关于RSV疫苗振奋人心的消息不止如此,就在昨天,医药巨头阿斯利康(AstraZeneca)以11亿美金收购美国上市的疫苗厂商Icosavax。 结合国际上已商业化的两款RSV疫苗首季度表现(12亿美金销售),和阿斯利康11亿美金大手笔并购新闻,当前态势愈发明晰:进入临床阶段重组蛋白路线的RSV PreF疫苗研发前景被业界高度认可,相应的,日后其市场空间也不可估量。这种“高度稀缺性”侧面反映出“已进入临床阶段重组蛋白路线的RSV PreF疫苗”这条技术细分赛道并不拥挤,除了产品已获批的GSK和辉瑞,以及刚被阿斯利康收购的Icosavax,目前全球范围内,拥有进入临床阶段重组蛋白路线RSV PreF疫苗的只有三叶草生物。
"我们很高兴成为中国首家开发 RSV PreF (基于融合前构象的F蛋白) 疫苗并进入人体临床试验阶段的疫苗公司,这坚定了三叶草生物在RSV疫苗领域的领跑地位,也证明了我们已经验证的 Trimer-Tag 疫苗技术平台的创新价值和我们研发团队的强大实力",三叶草生物首席执行官兼执行董事梁果先生表示,"RSV 病毒感染疾病负担沉重,RSV疫苗用于防治的需求缺口巨大;目前在中国本土的疫苗厂商中,迄今为止除三叶草生物的此款RSV PreF候选疫苗外,还没有任何一款RSV PreF(基于融合前构象的F蛋白)疫苗进入临床试验阶段,而全球范围内也有差异化竞争的机会。”
三叶草生物对其候选疫苗的自信并非空中楼阁,其RSV候选疫苗SCB-1019在临床前试验中展现出的四个特点值得细说:
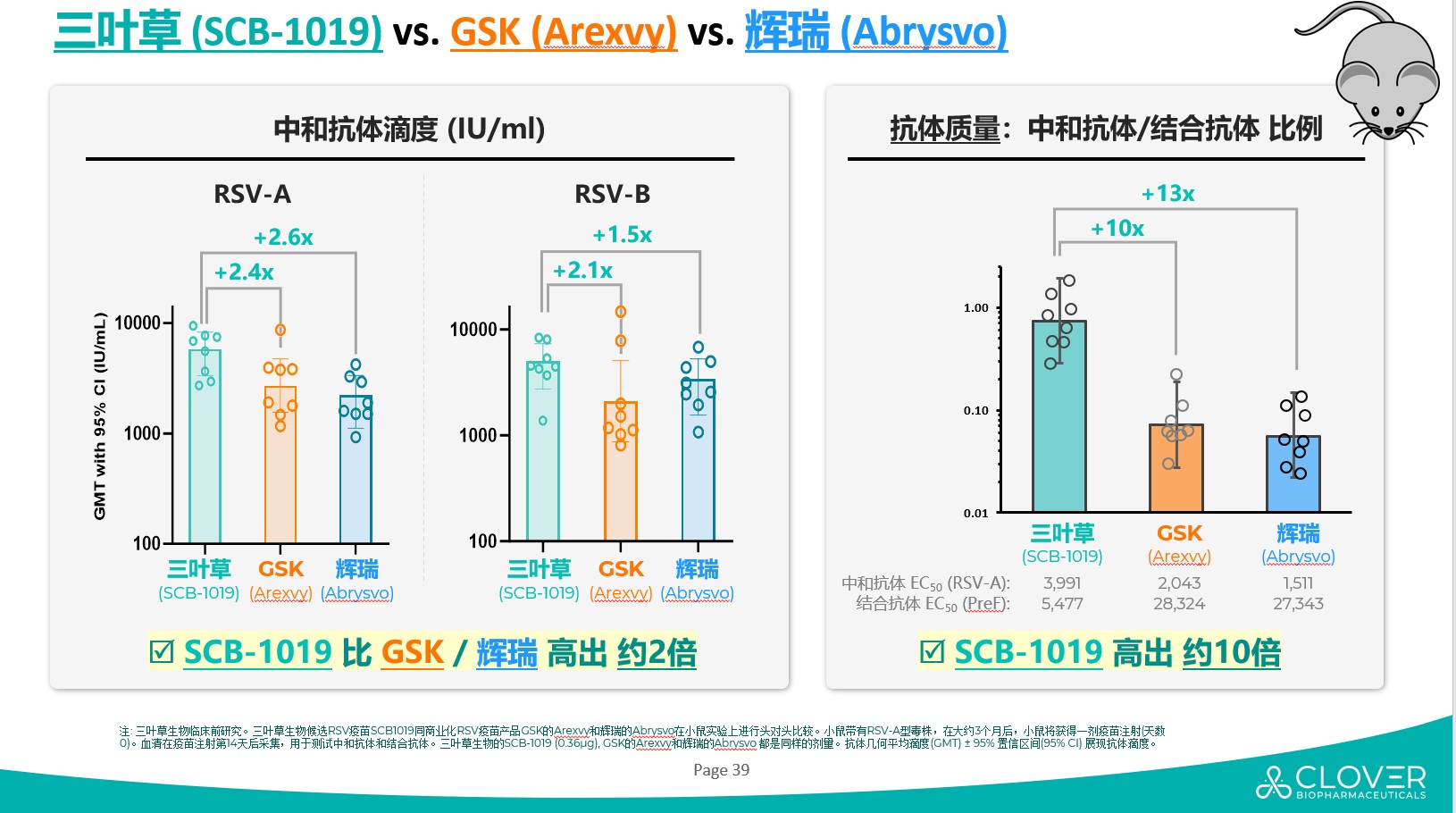
首先,临床前数据显示SCB-1019能诱导更强和更高质量的中和抗体:在临床前试验中头对头比较已商业化的两款RSV疫苗,SCB-1019展现了更高的中和抗体和更高质量的抗体水平。在免疫原性实验中,同等剂量情况下,SCB-1019诱导的针对A和B两个RSV株系的中和抗体水平都是已商业化两款RSV疫苗的约2倍;同时SCB-1019诱导的中和抗体比值超过两个已商业化RSV疫苗约10倍。显示出SCB-1019有潜质成为全球更高效的候选RSV疫苗竞品。
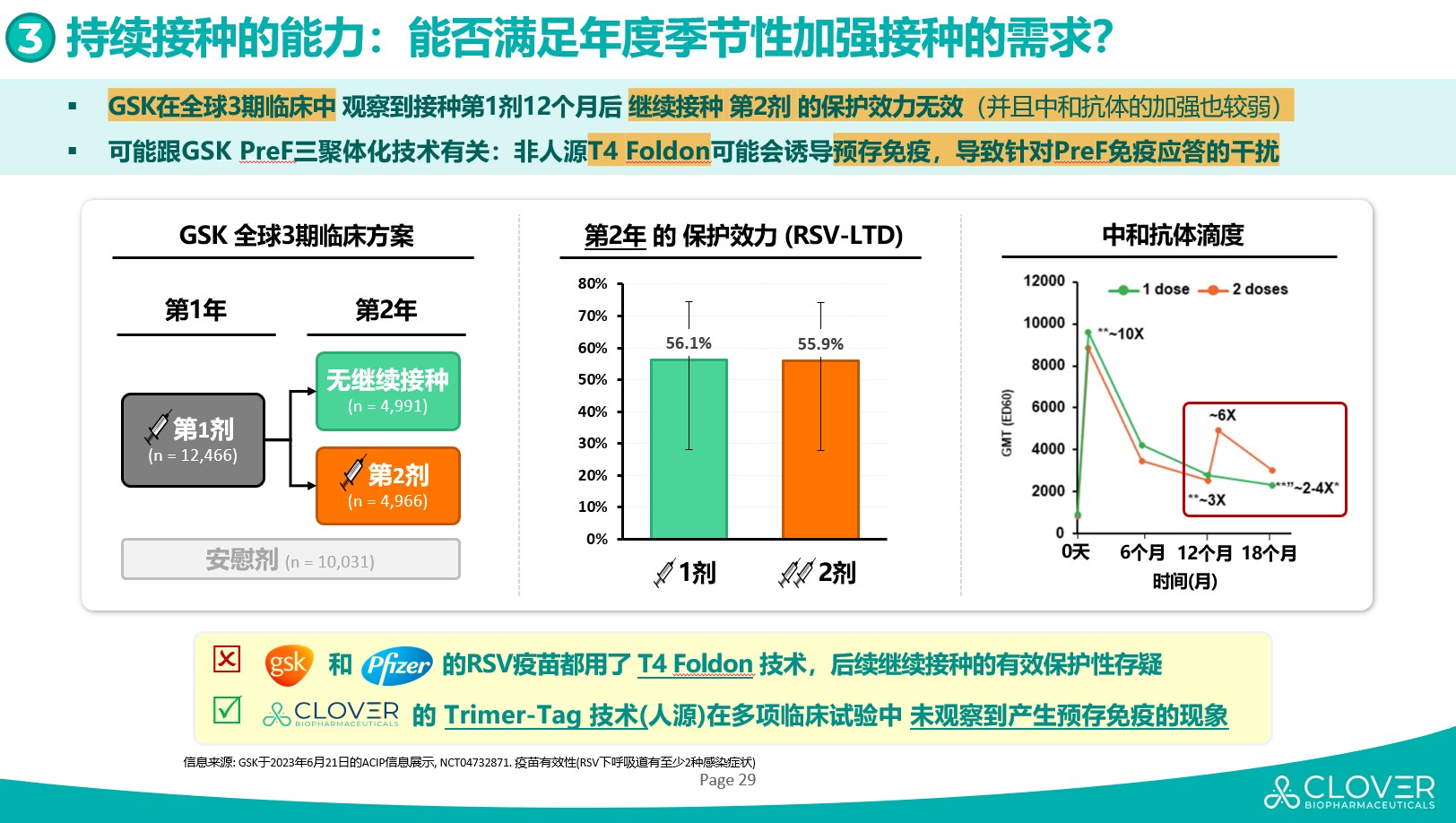
其次,SCB-1019候选疫苗预计不会诱导预存免疫,有望满足年度、季节性重复接种的需求。与季节性流感疫苗类似,RSV疫苗也需要每年重复接种,因此年度、季节性接种对RSV感染的有效保护不言而喻。目前有已获批的RSV疫苗可能因为技术原因诱导了预存免疫,则可能导致后续接种无效。例如GSK获批的单价RSV-A疫苗Arexvy,在其全球III期临床试验中,观察到接种第1剂12个月后,继续接种第2剂的保护效力无效,且很难诱导其中和抗体水平增强。这可能同其三聚体化技术有关,因为非人源的T4Foldon可能会诱导预存免疫,导致针对融合前F (PreF) 免疫应答的干扰。据了解,辉瑞的RSV疫苗Abrysvo也采用了非人源的T4Foldon技术,难免存在相同的问题。
三叶草生物的RSV候选疫苗SCB-1019得益于全人源的蛋白质三聚体化(Trimer-Tag)技术,基于过往开发疫苗的多项临床试验经验,未曾观察到产生预存免疫的现象,因而极具潜力可满足RSV疫苗需要年度、季节性加强的接种需求。
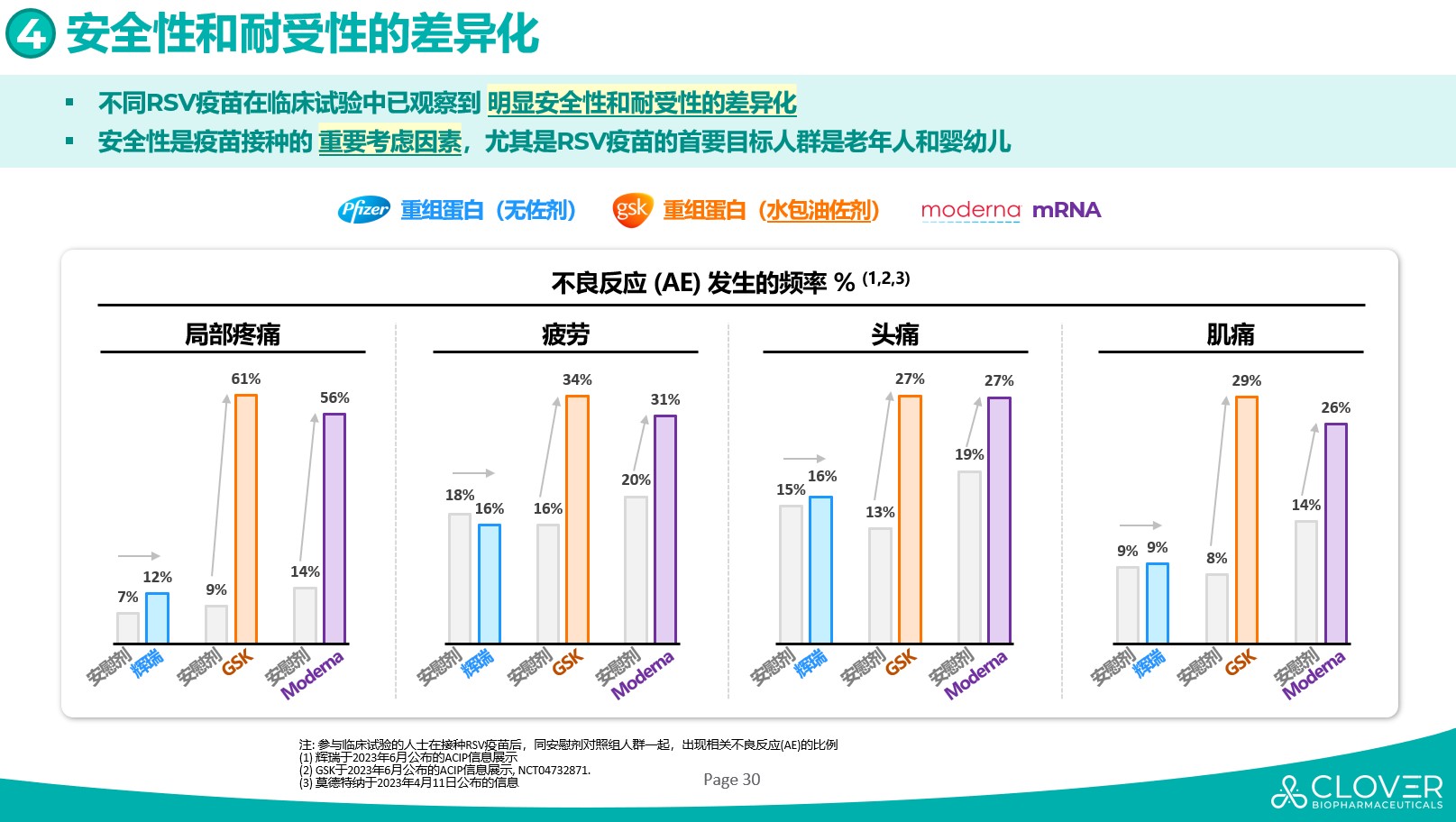
第三,安全性是疫苗接种的重要考虑因素,尤其RSV疫苗的主要目标人群是老年人和婴幼儿。辉瑞、GSK(使用了水包油乳化佐剂)和Moderna不同厂商的RSV疫苗产品在临床试验中已观察到明显安全性和耐受性的差异,而三叶草生物的SCB-1019将不采用水包油乳化佐剂,或可显示优异的安全性和耐受性特点,有望具备潜在行业最佳的安全性和耐受性。考虑到RSV疫苗最主要的接种目标群体是老年人和婴幼儿,RSV疫苗的安全性和耐受性从某种程度上而言,可能比高效的保护性更重要,这也直接影响了产品后续的商业化空间。
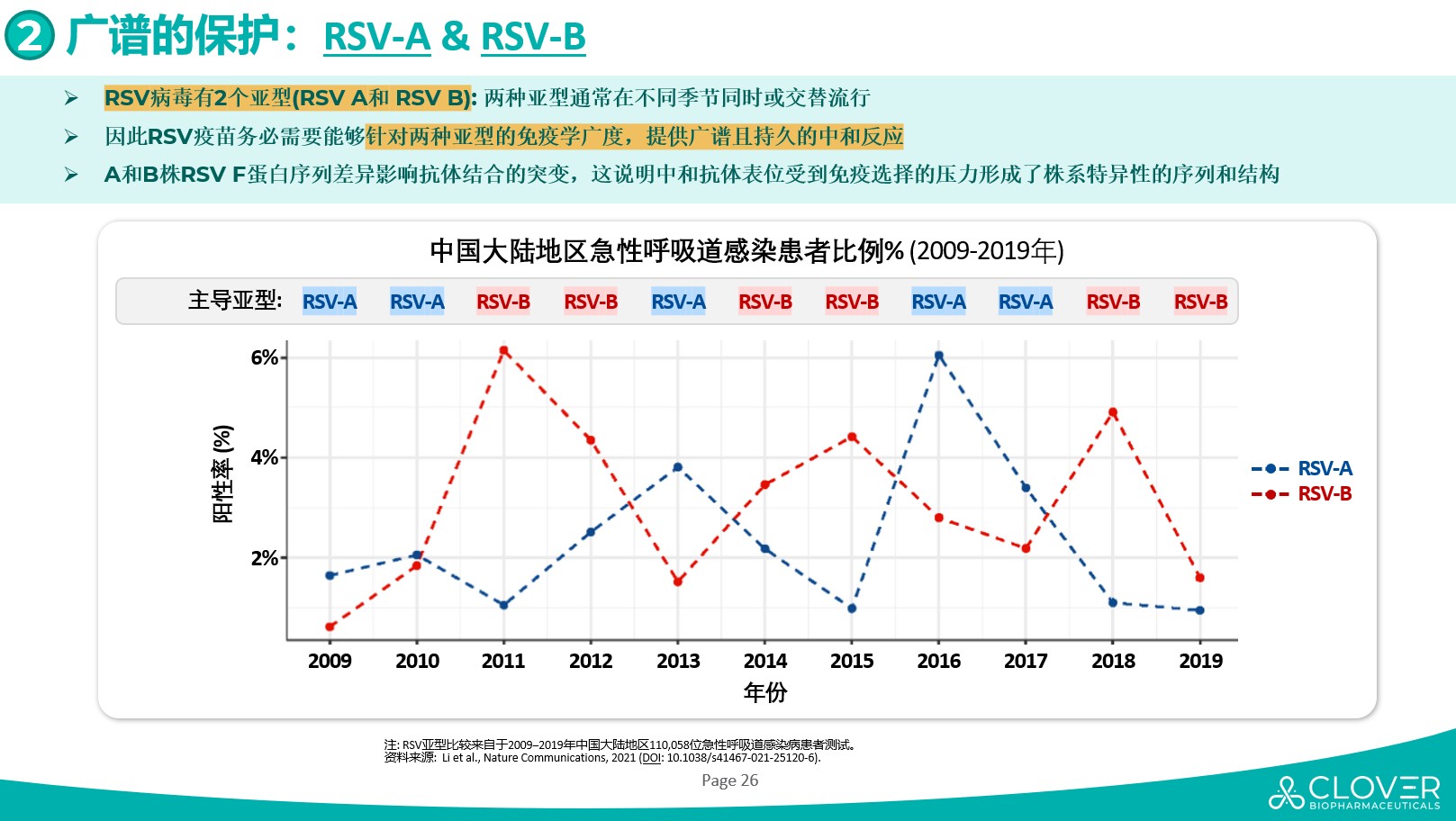
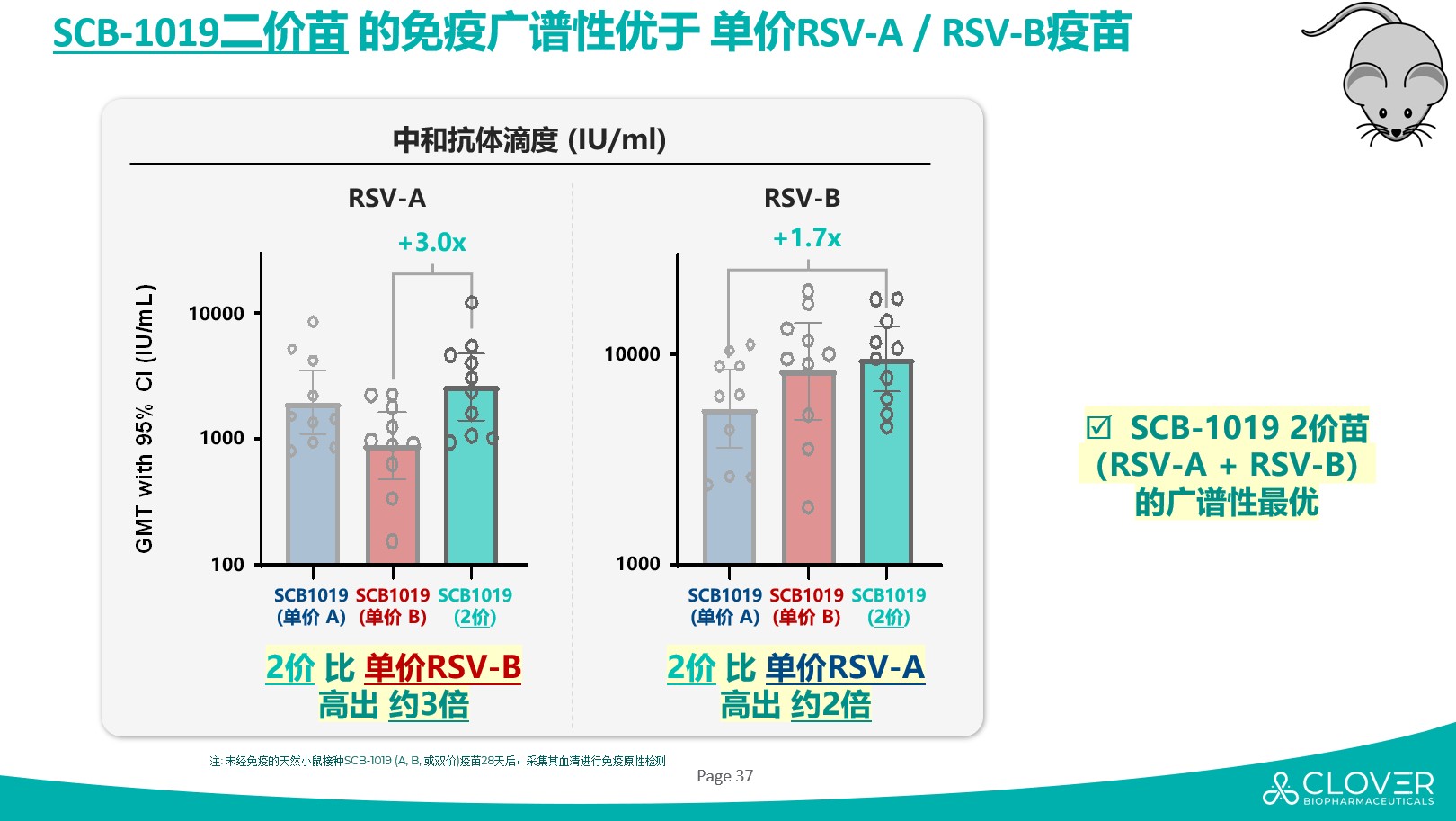
最后,二价RSV疫苗有更好的免疫广谱性。RSV病毒有A和B两个亚型,在流行季通常出现A和B交替或同时流行的现状。GSK获批的单价RSV-A疫苗Arexvy在其III期临床试验中观察到针对RSV-B的保护力和保护持久性较差。同时Icosavax的单价RSV-A疫苗也在其全球Ib期临床中也同样观察到针对RSV-B的中和抗体水平和其持久性较差。 因此,高效的RSV疫苗必须具备能够针对两种病毒亚型的免疫学广度,并能诱导产生广谱且持久的中和反应。作为一款二价重组蛋白RSV候选疫苗,三叶草生物RSV PreF候选疫苗SCB-1019的临床前数据已经展现了优秀的免疫广谱性。
除此之外,SCB-1019的生产使用了与三叶草生物的新冠疫苗相同的蛋白质三聚体化(Trimer-Tag)技术平台,并计划在三叶草生物的长兴工厂进行商业化生产。该工厂已通过多次GMP核查,并已获得中国国家药监局颁发的疫苗药品生产许可证(DML),产能实力可满足市场需求。这确保了三叶草生物与其他使用新生产基地的国内疫苗生产商相比,具有明显优势。
虽然国际上有两款RSV疫苗获批, 但国际厂商的RSV疫苗进入中国实现商业化可能还需要至少3年时间。中国本土疫苗企业在RSV疫苗的开发方面虽然刚起步,但就像三叶草生物一样,相信都会全速推进自研RSV疫苗的临床工作。据悉,三叶草生物于澳大利亚启动的Ⅰ期临床试验是一项随机、安慰剂对照的研究,目的是评估 SCB-1019 在年轻成年人和老年人群体中不同剂型、不同剂量水平下的安全性、反应原性和免疫原性。三叶草生物表示,其安全性和免疫原性结果预计于 2024 年下半年公布,期待更多的临床进展。
作为一家处于商业化阶段的全球生物制药公司,三叶草生物致力以创新型疫苗拯救生命和改善全球健康水平,当下专注于打造领先的呼吸道疫苗产品组合,以解决在预防严重的呼吸道感染疾病领域未被满足的需求,同时把握相关重要的交叉推广、联合配给和长期生命周期管理机会。除了自研的呼吸道合胞病毒(RSV)疫苗,已经商业化的四价季节性流感疫苗,三叶草生物还在继续扩充其中后期疫苗管线并优先考虑其他呼吸道疫苗产品,寄望以丰富的疫苗产品组合,帮助构建免疫屏障,护佑千万家庭。
