在对医药企业进行估值时,研发管线的稀缺性、潜在的市场前景、药物的疗效和安全水平,都是重要的考量因素。随着重磅大单品LuX-Valve经导管三尖瓣置换系列产品在全球获得积极进展,健世科技-B(09877)频频获得券商投行等机构多方唱好。
具体而言,中金公司给予跑赢行业评级,目标价45港元,称健世科技为三尖瓣介入全球领军企业,公司收入有望从2024年开始快速放量;花旗对健世科技给予“买入”评级,目标价40港元,并指出现有股价相较于IPO价格处于低估值区间;华安证券首次覆盖并给予“买入”评级,预计公司将在2025年实现6.19亿元的营业收入,看好其迅速商业化带来营收突破的能力以及大单品全球化预期。
重磅产品商业化在即,多重利好催化市场预期上行,步入收获期的健世科技后市将迎来多大的想象空间?
国产自研医械商业化积极推进 临床数据表现亮眼
近期LuX-Valve经导管三尖瓣置换系统的确证性临床试验一年期结果,在2023年伦敦心脏病瓣膜病介入治疗会议(PCR London
Valves)上正式发布。
三尖瓣反流是由三尖瓣无法完全闭合引起的,由于三尖瓣解剖结构复杂,且患者多为高龄老年人,开胸手术风险相对较高,多年来接受外科手术的三尖瓣病变患者住院期间死亡率持续居于高位。
据智通财经APP了解,目前临床上对于瓣膜性产品疗效的评估主要有三个维度:患者心功能改善、反流和瓣周漏降低与患者身体状况提升。而LuX-Valve和Lux-Valve
Plus均展现了亮眼的临床数据。
本次LuX-Valve确证性临床研究共纳入126例重度三尖瓣返流患者,旨在评估LuX-Valve经导管三尖瓣置换系统在重度三尖瓣反流患者中的安全性和有效性,临床试验主要终点为术后一年累积全因死亡率。临床试验一年访问数据显示,根据超声数据,99.1%的患者三尖瓣反流等级得到改善,94.4%的患者三尖瓣反流分级降低至轻度及以下,75.7%的患者恢复至无/微量三尖瓣反流。
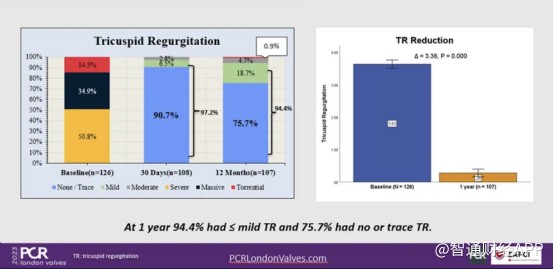
(资料来源:健世科技官方公众号)
从安全性指标看,一年全因死亡率9.6%(PPS集,植入瓣膜的患者中);肾功能和肝功能衰竭发生率分别为4.0%和2.4%,III度房室传导阻滞或需要安装永久性起搏器发生率仅为1.6%,术中转外科手术换瓣或成形0.8%,卒中2.4%,数据显示患者术后并发症低,安全性得到有效验证。
从有效性指标看,在随访30天时,66.3%的患者NYHA心功能由III / IV级改善至I / II级,在随访一年时,79.8%的患者由术前III /
IV级改善至I /
II级;此外,6MWD(6分钟步行距离)在随访30天时,Lux-Valve由基线324.3米提升9.3米至333.6米,在随访一年时即提高至383.2米。
与此同时,二代产品LuX-Valve
Plus经血管三尖瓣置换系统的多中心临床试验结果也于近期在2023年美国经导管心血管治疗大会(TCT)正式发布。本次临床试验共纳入96例患者,所发布的一个月临床数据终点为手术后30天复合事件发生率。随访30天数据显示,根据超声数据,100%患者三尖瓣反流等级得到改善,97.81%的患者三尖瓣反流分级降低至无或者微量。

(资料来源:健世科技官方公众号)
安全性结果显示,Lux-Valve Plus
30天复合不良事件发生率仅为6.45%。同时,心肌梗死、卒中、使用ECMO或IABP、急性肝功能衰竭、长期机械通气(>72小时)、需要外科干预的心血管损伤(心脏穿孔、血管损伤)、危及生命的大出血事件发生率均为0;全因死亡率仅为1.08%且与器械无关。
有效性结果显示,随访30天数据下,100%的患者三尖瓣反流降低至轻度及以下,92.31%的患者显示无或仅微量瓣周漏;80.43%患者由术前NYHA III
/ IV级提升至I / II级。至于6MWD(6分钟步行距离),Lux-Valve Plus患者提升了12米。
三尖瓣介入置换术式因三尖瓣解剖结构的复杂性而大幅提升了介入瓣膜的研发难度,全球范围内仅健世科技的LuX-Valve系列产品与美国爱德华生命科学(EW)的EVOQUE产品进度领先。LuX-Valve与LuX-Valve
Plus经导管三尖瓣置换系统通过独特的“室间隔锚定”人工瓣膜固定方式及“自适应防漏环”设计,有效突破三尖瓣重度反流患者的临床痛点和治疗难点。其中,“自适应防漏环”的设计可以有效降低瓣周漏的发生,不会对三尖瓣周围组织产生压迫,更有利于术后的心功能恢复;全球首创的“室间隔锚定”设计则利用特殊的于室间隔上受力锚定和夹持件结构,从根源上解决人工瓣膜难以固定在心腔内的难题。
值得关注的是,爱德华也同样于近期披露了其EVOQUE经导管三尖瓣置换系统的TRISCEND
II研究中接受治疗的患者的临床结果。参加研究的患者同时接受了最佳的药物治疗,临床数据显示一定比例的中度或高度功能性或退行性三尖瓣反流(TR)的情形依然存在。根据其公布的数据,EVOQUE搭配最佳药物治疗的30天复合不良事件发生率为27.4%。随访6个月数据下,67.4%的患者NYHA心功能由III
/ V级改善至I / II级(排除掉治疗前基线数据中本来就有22.6%的患者是I /
II级);93.8%患者的反流程度降低至轻度及以下,其中77.8%的患者显示无或仅微量瓣周漏。6MWD(6分钟步行距离)在随访30天时出现了下降,随后在6个月随访中回升。
从数据对比中可以看出,健世科技的一代产品LuX-Valve和二代产品LuX-Valve
Plus在安全性、有效性与患者长期身体状况恢复的方面都具备明显优势、拥有全球领先的水平。期待更长期的临床数据持续公布。
此外,三尖瓣置换临床治疗时,常存在外科手术高危的极重度三尖瓣反流(TR)患者因瓣环极大而无法采取介入治疗的情况。而LuX-Valve覆盖的最大瓣环直径达65-75mm,远高于EVOQUE的最大瓣环直径52mm,具有更广阔的适应症范围。
据报道,近期健世科技的二代三尖瓣置换产品LuX-Valve
Plus在亚太地区多家医院成功完成了一系列收费同情救治使用,其中包括数例罕见复杂解剖结构的病例。术后患者临床表现、心脏功能及生活质量显著改善,已然充分证明了该产品具有适用范围广、可靠性高及操作简单的优异性能。
心脏瓣膜赛道“分秒必争” 健世科技研发进度稳居第一梯队
心血管疾病是医药行业最具潜力的领域之一。据智通财经APP了解,近年来全球心血管疾病患者群体庞大,且患病率持续上升。《中国心血管健康与疾病报告2022概要》中指出,在我国城乡居民疾病死亡构成比中,心血管疾病(CVD)占首位。而在心血管病分类中,瓣膜性疾病手术量占比最高。
相比主动脉瓣与二尖瓣,三尖瓣的瓣叶更薄、更脆弱,其复杂的结构也增加了介入治疗的难度。根据美国流行病学资料,三年三尖瓣反流(TR)重度患者死亡率高达50%。可以看出,三尖瓣介入治疗市场尚处于早期阶段,存在巨大的治疗缺口。
国家经导管瓣膜治疗数据库(NTCVR)数据显示,截至2022年底,中国大陆地区已累计进行了23980例经导管主动脉瓣置换术(TAVR)手术,而到2023年10月31日累计手术数量达到35594例,呈现逐年增长的趋势;根据Frost&Sullivan预测,中国的经导管三尖瓣介入治疗(TTVI)市场预计在2023年达到8560万元人民币,到2030年将增至203亿元,年复合增长率(CAGR)为118%。

2010-2023年中国大陆地区TAVR手术例数(图源:瓣膜中心,数据来源:NTCVR)
不同于许多成熟的医疗领域,由外资品牌占主导,面对这片广阔的待掘蓝海,国内企业与外资企业正站在同一条起跑线上,可以说谁能在这场军备竞赛中“抢占”研发高地,谁就有望凭借商业化的快速放量分得更多市场份额。
在三尖瓣介入治疗中,有着介入置换(TTVR)与介入修复(TTVr)两条不同的细分技术路径。与经导管三尖瓣修复相比,经导管三尖瓣置换的潜在目标患者群体更广泛,对患者原生瓣膜情况的限制也较少。
截止目前,全球仅有4款修复产品获CE认证,包括缘对缘修复(T-TEER)路径的雅培TriClip、爱德华PASCAL,瓣环成形路径的爱德华Cardioband和异位置换路径的德国PF
TricValve,而原位置换路径下尚无获批产品。不过,即使有多款修复产品问市,经过多年临床实践,手术量依然有限,说明了介入修复手术在治疗三尖瓣反流疾病上是有着明显的局限性,近期亦有海外文献证明此点。在三尖瓣置换领域,全球研发进度领先的为健世科技自主研发的LuX-Valve一代和二代产品以及爱德华公司的EVOQUE。
具体而言,健世科技的一代产品LuX-Valve已经完成了确证性临床并进入了国家药监局(NMPA)注册审查阶段,预计将于近期获批,率先一步进入经导管三尖瓣置换(TTVR)中国市场。
二代产品LuX-Valve Plus则已完成NMPA的确证性临床试验临床数据展现了极佳的安全性和有效性。
此外,LuX-Valve Plus在北美临床及商业化进程加速,已在包括美国及加拿大等在内的北美地区完成数十例临床植入;LuX-Valve
Plus的早期可行性研究(EFS) pre-submission申请已获美国食品及药物管理局(FDA)正式受理。在欧洲多个国家的临床中心快速推进CE
MARK注册临床试验入组。
对此,华安证券指出,预计健世科技的产品进度领先于国内同行的同类产品至少3年。重磅产品进入研发第一梯队,无疑将使得健世科技在商业化窗口期充分享受市场红利,叠加公司丰富的管线布局,有望为业绩带来持续高增长动力。
多条技术路径齐头并进 着力打造全覆盖产品矩阵
基于对结构性心脏病的深刻理解,健世科技已拥有丰富的产品矩阵,成为国内唯一一家对结构性心脏病实现全覆盖的企业。目前公司共有12款产品正处于临床与注册阶段,其中包含8款心脏瓣膜产品、2款心力衰竭产品与2款心源性卒中防护产品。
在二尖瓣介入治疗领域,目前全球范围内并无完全成熟的治疗方案,而健世科技通过同时研发修复、局部置换以及全瓣置换这三种完全不同的技术路径,将在未来实现更为广泛的患者临床需求覆盖。
目前,公司二尖瓣产品布局包括创新经导管二尖瓣修复夹持系统JensClip、使用瓣叶修补技术修复二尖瓣的MitraPatch、二尖瓣瓣叶增强系统JensFlag和二尖瓣全瓣置换系统JensRelive等。
除了三尖瓣领域的两款LuX-Valve核心产品,公司还研发了针对主动脉反流适应症的产品Ken-Valve,预期将成为全球市场第三款和中国市场第二款适应症可同时覆盖主动脉瓣关闭不全(或合并主动脉瓣狭窄)的产品。
近日,Ken-Valve的注册申请获批进入国家药监局(NMPA)的医疗器械优先审批程序,其同时也成为国家药监局开通优先审批通道后,首个于心脏瓣膜领域获选进入优先审批程序的产品。纳入优先审批程序后,产品获批速度将大幅提升,商业化进程加速。
除了瓣膜业务外,健世科技在治疗心衰、心源性卒中防护领域方面亦有多款产品布局,如自主研发的心房间隔造孔支架及输送系统MicroFlux,及左心耳封堵器系统SimuLock与PFO封堵器系统OmniSeal两款心源性卒中防护产品,其中SimuLock已成功完成多例注册临床FIM入组。
展望未来,随着多款产品密集商业化落地,中国市场及海外市场将双重驱动健世销售收入可持续高增,而公司在结构性心脏病研发布局上的“全面开花”亦将提升抗风险能力,增厚后续业绩的确定性。在医药行业更加聚焦独创性与国际化的当下,有丰富产品储备傍身的健世科技已然具备充分的上行动能。亦期待有更多的中国自主创新的医疗器械能够在细分领域实现“弯道超车”。
